Bộ Y tế thu hồi 11 loại thuốc có chứa tạp chất nguy cơ gây ung thư
GiadinhNet - Bộ Y tế thu hồi 11 loại thuốc có Ranitidine do phát hiện chứa tạp chất NDMA có nguy cơ gây ung thư ở hàm lượng vượt quá ngưỡng cho phép.
Cục Quản lý Dược (Bộ Y tế) cho biết, căn cứ vào các quy chế dược hiện hành của Việt Nam; căn cứ thông báo của Cơ quan Khoa học y tế Singapore (HSA), Cơ quan quản lý dược phẩm Thụy Sĩ (Swissmedic) về việc thu hồi các thuốc chứa Ranitidine do phát hiện chứa tạp chất N-nitrosodimethylamine (NDMA) có nguy cơ gây ung thư ở hàm lượng vượt quá ngưỡng cho phép của quốc tế.
Để đảm bảo an toàn cho người sử dụng, Cục Quản lý Dược yêu cầu thu hồi tất cả các thuốc thành phẩm có tên sau đây:
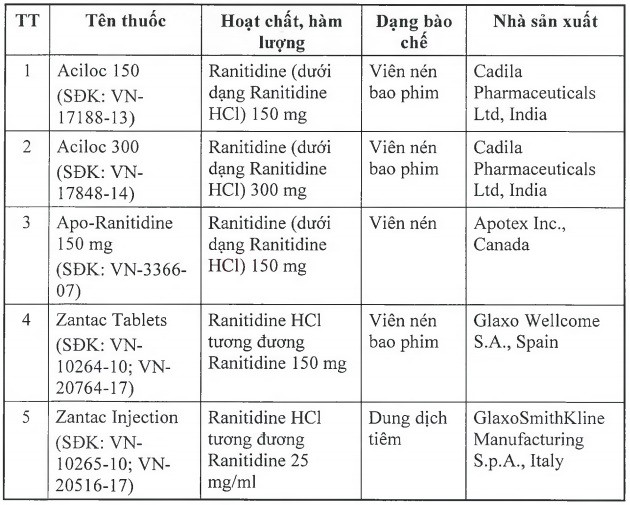
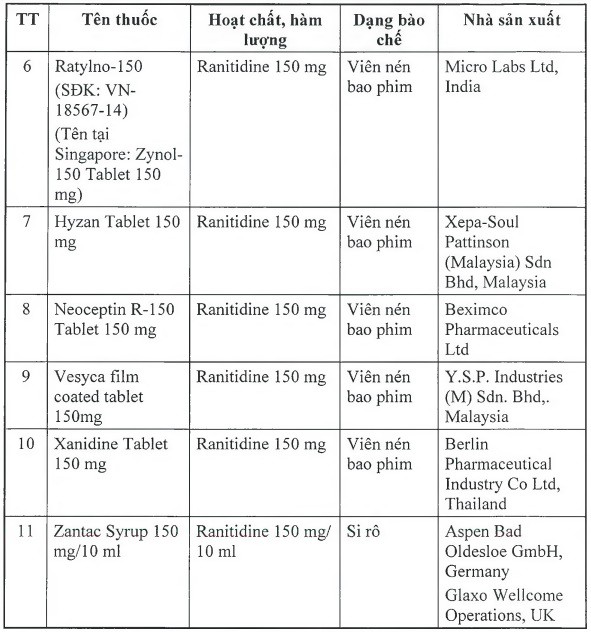
Cục Quản lý Dược yêu cầu các Công ty nhập khẩu thuốc phối hợp với nhà phân phối thuốc thông báo thu hồi tất cả các lô thuốc thành phấm nêu trên tới các cơ sở bán buôn, bán lẻ, sử dụng thuốc và tiến hành thu hồi toàn bộ các lô thuốc này; Sở Y tế các tỉnh, thành phố phải thông báo việc thu hồi tới các cơ sở kinh doanh, sử dụng thuốc trên địa bàn. Kiểm tra và giám sát các Công ty nhập khẩu thuốc trên địa bàn thục hiện việc thu hồi các thuốc nêu trên.
Cục Quản lý Dược yêu cầu các cơ sở nhập khẩu thuốc, nguyên liệu dược chất Ranitidine thực hiện nghiêm túc việc đánh giá cơ sở cung cấp, cơ sở sản xuất nguyên liệu, cơ sở sản xuất thuốc thành phẩm.
Cơ sở nhập khẩu nguyên liệu chỉ nhập khẩu các lô nguyên liệu Ranitidine đạt tiêu chuẩn chất lượng theo tiêu chuẩn đã được chấp nhận, đồng thời không có hoặc không vượt quá giới hạn cho phép các tạp chất NDMA. Cơ sở nhập khẩu chịu trách nhiệm lưu trữ các bằng chứng chứng minh lô nguyên liệu nhập khấu đáp ứng yêu cầu trên.
Cơ sở nhập khẩu thuốc phải phối hợp với cơ sở sản xuất thuốc nuớc ngoài đảm bảo thuốc chứa dược chất Ranitidine được sản xuất từ nguồn nguyên liệu không có hoặc không vượt quá giới hạn tạp chất NDMA. Cơ sở nhập khẩu thuốc chịu trách nhiệm về việc lưu trữ các bằng chứng chứng minh từng lô thuốc nhập khẩu đạt tiêu chuẩn chất lượng và được sản xuất từ lô nguyên liệu dược chất Ranitidine đáp ứng yêu cầu nêu trên.
Song song với công văn yêu cầu thu hồi 11 loại thuốc thành phẩm chứa Ranitidine trên đây, ông Đỗ Văn Đông, Phó Cục trưởng Cục Quản lý Dược cũng có công văn đề nghị Viện Kiểm nghiệm thuốc Trung ương, Viện Kiểm nghiệm thuốc TP HCM nghiên cứu, triển khai và hướng dẫn các Trung tâm kiểm nghiệm tỉnh, thành phố thực hiện quy trình phân tích xác định tạp chất NDMA trong nguyên liệu và trong thuốc chứa dược chất Ranitidine.
Tăng cường lấy mẫu để kiểm tra chất lượng nguyên liệu và thuốc chứa dược chất Ranitidine tại cơ sở nhập khẩu và cơ sở sản xuất thuốc, và ưu tiên phân tích bổ sung xác định tạp chất NDMA trong mẫu đã lấy.
Võ Thu
Bỗng dưng mờ mắt, phát hiện khối phình động mạch não "khổng lồ"
Y tế - 2 giờ trướcSau khi lần lượt mờ 2 mắt, với thị lực gần như bằng 0, đi qua rất nhiều bệnh viện khám, nữ bệnh nhân ở Quảng Bình được xác định có khối phình động mạch não rất lớn.
Bé 3 tuổi bị que xiên thịt đâm xuyên lưỡi
Y tế - 6 giờ trướcGĐXH - Bệnh nhi nhập viện trong tình trạng chiếc que xiên thịt sắc nhọn đâm xuyên lưỡi.
Nam sinh lớp 8 bị đánh chấn thương sọ não hiện ra sao trong thời gian điều trị tại BVĐK Phú Thọ
Y tế - 13 giờ trướcGĐXH - Về tình hình sức khỏe của nam sinh bị đánh chấn thương sọ não khi chơi bóng rổ, đại diện Bệnh viện Đa khoa tỉnh Phú Thọ cho biết hiện tại, bệnh nhân vẫn hôn mê, thở hoàn toàn theo máy...
Sau bữa cơm cá, người phụ nữ ho, khó thở suốt 1 năm
Y tế - 4 ngày trướcXương cá rơi vào phế quản nhưng bà K.A không hề hay biết. Bị ho, khó thở kéo dài, bệnh nhân điều trị suốt 1 năm không đỡ.

Hội thảo báo cáo về kết quả khảo sát tính khả thi việc triển khai chương trình đào tạo nhân lực phục hồi chức năng tại Việt Nam
Y tế - 4 ngày trướcGĐXH - Ngày 19/4 tại Hà Nội đã diễn ra Hội thảo báo cáo về kết quả khảo sát tính khả thi việc triển khai chương trình đào tạo nhân lực phục hồi chức năng tại Việt Nam do JICA phối hợp với Hội Vật lý Trị liệu Việt Nam tổ chức.

Bộ Y tế: Hàng trăm cán bộ ngành Y hiến máu cứu người hưởng ứng ‘Lễ hội Xuân hồng’ năm 2024
Y tế - 5 ngày trướcGĐXH – Hàng trăm đơn vị máu đã được tiếp nhận trong Chương trình hiến máu tình nguyện hưởng ứng “Lễ hội Xuân hội’ năm 2024 tại Bộ Y tế.

Hà Nội phát động tháng An toàn vệ sinh lao động, gần 200 công nhân được khám sức khỏe miễn phí
Y tế - 5 ngày trướcGĐXH - Ngày 19/4, UBND TP Hà Nội và Liên đoàn Lao động thành phố phát động Tháng hành động về An toàn, vệ sinh lao động và Tháng Công nhân năm 2024.
Chơi đùa cùng bạn ở lớp, bé trai ở Hà Nội bị kính cứa đứt 2 cổ tay
Y tế - 5 ngày trướcGĐXH – Bệnh nhi bị đứt toàn bộ động mạch trụ, đứt thần kinh trụ và thần kinh giữa, đứt gân gấp cổ tay trụ, đứt gân gấp ngón 4 và 5 bàn tay trái.

Chó chết sau khi cắn chủ nhà, chuyên gia giải thích vì sao chó dại sau khi cắn người lại chết?
Y tế - 5 ngày trướcGĐXH - Thực tế, kông phải việc cắn người sẽ khiến chó dại bị chết mà thực chất đây là biểu hiện xuất hiện vào giai đoạn cuối cùng trong quá trình phát bệnh của chó.
Bé gái chào đời với dây rốn quấn cổ 5 vòng
Y tế - 1 tuần trướcBé gái nặng gần 3 kg, có dây rốn quấn cổ 5 vòng, ngôi ngược vừa được các bác sĩ phẫu thuật mổ lấy thai thành công
Thông tin mới nhất vụ thanh niên ngừng tim trước vạch đích giải chạy Tây Hồ: Có tiền sử tăng huyết áp
Y tếGĐXH - Bệnh nhân có tiền sử tăng huyết áp 4 năm, thường xuyên được điều trị bằng Coversyl.